Kalcium-dinátrium-etiléndiamin-tetraacetát (Ca-Na-EDTA) (E385)
(Calcium disodium EDTA)
Az etiléndiamin-tetraecetsav (EDTA) ill. sói (amiket edetátoknak is hívnak) igen jó komplexképző, kelátképző anyagok: nagyon könnyen megkötik az oldatban levő nehézfém ionokat – mint a lentebbi ábrákon is látható, a négy savcsoport és a két nitrogén atom szorosan körülöleli az ionokat és nem engedi más anyagokkal reagálni. Ezt a tulajdonságát a kémiában, analitikában sokfelé hasznosítják. Az élelmiszereknél is erre használják, pl. fémdobozban levő konzerveknél, vagy minden olyan esetben, amikor nehézfémek szennyezhetik az anyagot. A nehézfémek, mégha csak ártalmatlan nyomnyi mennyiségben is vannak jelen, elszíneződést okozhatnak, nem kívánatos oxidációt katalizálhatnak stb. Az orvosi gyakorlatban a kalcium-EDTÁ-t nehézfém mérgezésekben használják életmentőként. A nátrium-EDTA lecseréli a vízben levő kálciumot nátriumra, lágyítja a vizet, ezért szappanokhoz és hasonló kozmetikai készítményekhez is szokták keverni.
Maga az EDTA ártalmatlan, mivel azonban a nemkívánatos fémeken túl megkötheti a hasznos nyomelemeket is, csak indokolt esetben és pontosan kiszámított mennyiségben szabad élelmiszerekben használni.

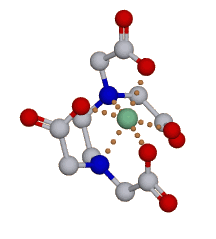
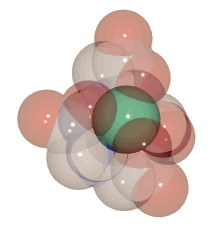
Az EDTA és egy nehézfém ion komplexének modelje. Az EDTA molekula hat oldalról szorosan körülveszi a fém iont és szinte elrejti, amint az a félig áttetsző térkitöltéses modellen jól látható. A komplexben megkötött fém ezután szinte szó szerint "angolosan távozhat" a szervezetből.